 流行病学
流行病学
流行病学:小肠淋巴组织较为丰富,是结外淋巴瘤的好发部位,在全部原发性胃肠道淋巴瘤中,以胃淋巴瘤最多(1/2),小肠其次(1/3),大肠淋巴瘤少见。国内统计小肠淋巴瘤占小肠恶性肿瘤的35.5%,刘宝华综合国内3830例小肠恶性肿瘤,
恶性淋巴瘤1505例,占39.3%,是我国第1位小肠恶性肿瘤。本病的发病年龄有两个高峰期,即15岁以前和40~60岁之间。男性多发,男女之比为2∶1。
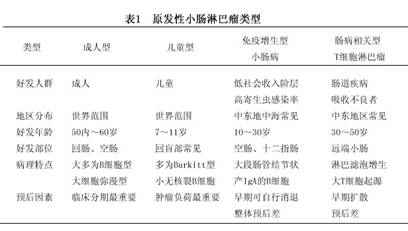
在发病类型上,在我国小肠淋巴瘤以成人型常见。而在儿童小肠恶性肿瘤中,儿童型淋巴瘤在国内外均占第1位。
 发病机制
发病机制
发病机制:
1.好发部位 小肠
恶性淋巴瘤一般起源于小肠黏膜下淋巴滤泡组织,向肠壁各层浸润。可发生于小肠任何部位,但由于远端小肠有较丰富的淋巴组织,故
恶性淋巴瘤多见于回肠(约50%),其次是空肠(30%),十二指肠最少(10%~15%)。
2.病理学 小肠原发性淋巴瘤绝大部分属非霍奇金淋巴瘤,常见类型是黏膜相关组织淋巴瘤(MALT淋巴瘤)。肉眼所见:肿块为孤立性或多发性,多发性又可分为弥漫性及散在性。弥漫性者可见黏膜皱襞弥漫增厚伴有小结节、小息肉状突出物,常累及一段肠管;孤立性者倾向于呈环形,可致肠腔狭窄。
小肠淋巴瘤大体所见可分为4型,即息肉型、溃疡型、动脉瘤型、浸润缩窄型。
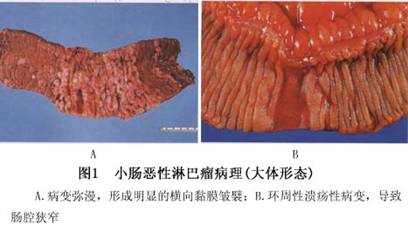
(1)动脉瘤型:最常见,沿肠壁黏膜下浸润生长,肠壁肌层及肠壁内神经丛受到损害,使肠壁增厚变硬,失去弹性而呈动脉瘤样扩张,故又叫囊样扩张型淋巴瘤。外观可见肿瘤环绕肠管,管壁僵硬呈皮革状,表面为暗红色或灰白色,黏膜常有多个结节样隆起,管腔呈扩张状态,由于肠壁高度增厚,可形成较大肿块(图1A)。
(2)浸润缩窄型:亦较常见,浸润肠壁引起增厚僵硬,蠕动消失,肠腔变窄,最后缩窄成很小内径。主要见于网状细胞肉瘤的病例,这种类型往往引起
肠梗阻。
(3)溃疡型较少见,溃疡位于浸润性肿瘤的中心部位,常为多发性,病变范围较小,但亦可是围绕肠腔的大溃疡,常易发生出血和穿孔(图1B)。
(4)息肉型:最少见,主要病变在黏膜下层,呈息肉状突入肠腔内,使黏膜皱襞消失,常为多发性病灶,最易发生肠套叠,故有人亦称之为息肉样肠套叠性淋巴瘤。
3.临床分期 根据肿瘤累及肠壁的深度及侵及范围,将
恶性淋巴瘤的病理过程划分为若干阶段,对临床预后的判断有重要指导意义。
(1)Contreary分期法:Ⅰ期:肿瘤局限于肠道,无转移;Ⅱ期:有肠系膜淋巴结受累;Ⅲ期:侵及主动脉旁或邻近器官。
(2)Mapvi分期法:Ⅰ期:肿瘤局限于肠管,病变为单灶性,无淋巴结转移;Ⅱ期:肿瘤累及邻近组织;Ⅲ期:肿瘤累及区域淋巴结;Ⅳ期:肿瘤广泛性浸润或远处转移。Ⅰ、Ⅱ期手术治疗预后较好。
4.转移途径 小肠
恶性淋巴瘤可通过直接蔓延、淋巴道或血道播散。肿瘤可沿肠壁浸润,也可穿透浆膜直接浸润肠系膜、大网膜、腹壁或邻近脏器,偶尔可穿透肠管而形成内瘘。
区域淋巴结转移是小肠
恶性淋巴瘤的主要转移方式,一般较腺癌早而且多见。最初至肠管周边的淋巴结,沿肠系膜淋巴管至区域淋巴结,然后至肠系膜根部淋巴结,晚期可转移至髂淋巴结、腹主动脉旁淋巴结甚至更远的淋巴结。淋巴结转移可为单发的,但常见为多个融合成团块状。
经血道转移较少,且多发生在较晚期,可至肝、胰、肾、肺、脑等脏器,以肝转移为最常见,可为单个结节或多个结节。
 其他辅助检查
其他辅助检查
其他辅助检查:
1.X线钡餐检查 尤其是小肠气钡双重造影是最重要的辅助检查。术前诊断率达30%~70%,一般可分为以下几种表现:
(1)弥漫性病变:病变范围广泛,全部小肠都可不正常。小肠正常黏膜皱襞大部分或全部消失,肠腔内可见到无数小的息肉样充盈缺损,由绿豆大至豌豆大,其大小约0.5~1cm直径。肠腔宽窄不一,沿肠壁可见到锯齿状切迹。胃内可见息肉或其他病变。
(2)多发性结节状充盈缺损,病变边缘清楚,黏膜纹紊乱、破坏或消失。
(3)狭窄性病变:中心性狭窄,其边缘僵硬,黏膜皱襞细如线条,狭窄的范围一般较长。偏心性狭窄,狭窄的一侧呈大块状充盈缺损突入肠腔使之变细,病变比较局限。外压性狭窄,肠腔变细并有外压现象,狭窄部位的黏膜皱襞仍然正常,病变范围较长,与正常小肠分界不清。狭窄近端肠腔扩张。
(4)扩张性病变:表现为肠腔不规则扩张,远超过肿瘤的范围,扩张段常与狭窄段相同,黏膜破坏、蠕动消失,肠壁僵硬,呈现动脉瘤样改变,小肠运动力减弱,数小时后,扩张肠管仍可见钡剂潴留。
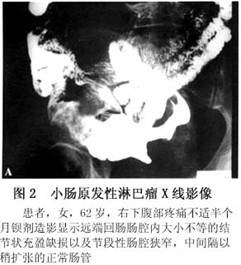
(5)肠套叠:呈现典型肠套叠X线表现,多由息肉样病变所致,套叠部位多位于小肠远端,最常见为回肠末端。上述征象可交错出现,结合临床常可作出诊断(图2)。
2.内镜检查 恶性淋巴瘤多发生于回肠末端,可用结肠镜检查,并可活检明确。内镜对于空肠上段的恶性淋巴瘤的诊断亦有帮助。
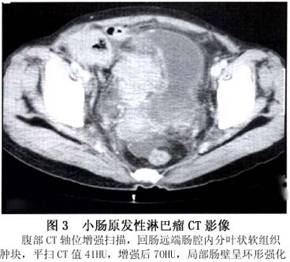
3.B超和CT 腹部肿块者,可见到肠管之间有结节状的团块。B超和CT帮助了解其位置,大小,与周围脏器的关系及有无淋巴结转移、肝转移、腹水等有参考意义。CT检查在肠腔内造影剂的对比下,可见肠腔有不规则的扩张或狭窄改变(图3),病变一般较广泛。但早期病变,难以确定。
4.手术探查 如经以上检查仍未明确诊断,应及早剖腹探查以达到诊断与治疗的目的。
 鉴别诊断
鉴别诊断
鉴别诊断:主要是与肠道炎性疾病中的克罗恩病、肠结核以及小肠癌相鉴别。
1.克罗恩病(克隆病) 可有节段性狭窄、卵石征或假息肉的征象,有时难与
恶性淋巴瘤相鉴别。但克罗恩病一般病史较长、常有复发史及肛周脓肿,可有
腹部肿块,往往因局部炎症穿孔形成内瘘,钡剂检查可见内瘘病变,节段性狭窄较光滑,近段扩张较明显,线性溃疡靠肠系膜侧,并有黏膜集中,肠袢可聚拢,呈车轮样改变。小肠
恶性淋巴瘤一般无内瘘形成,临床表现重,X线下狭窄段不呈节段性分布,边缘不光滑,结节大小不一,溃疡和空腔较大而不规则。
2.肠结核或腹膜结核 亦可出现腹部包块,有时与
恶性淋巴瘤较难鉴别,但前者一般都有结核病史,有低热、盗汗及血沉加快,腹部检查有揉面感,周身情况一般不出现进行性恶化,小肠结核X线见增殖型者表现为单发或多发的局限性肠腔狭窄,边缘较
恶性淋巴瘤光滑,近端扩张亦较明显;溃疡型者龛影一般与肠管纵轴垂直,
恶性淋巴瘤的溃疡部位不定,龛影较大而不规则。
3.小肠癌 病变往往局限,很少能触及包块,即使有亦是较小的局限的包块,X线钡餐检查仅为一处局限性肠管狭窄、黏膜破坏。
4.免疫增生性小肠疾病(IPSID) 是一种独特的小肠淋巴瘤,最初报道见于东方犹太人和阿拉伯人,又称为地中海淋巴瘤或α-重链疾病。典型的症状包括慢性
腹泻、脂肪泻,同时伴有呕吐和腹部痉挛性疼痛,亦可见杵状指。许多IPSID病人的一个少见的特点是,在血液和肠分泌物中,有一种异常的IgA,其α-重链缩短,且不含轻链。IPSID多发生于有肠内细菌及寄生虫感染的地区,有人认为,其病因可能与小肠内B淋巴细胞受肠内微生物抗原的长期反复刺激,引起细胞突变及恶变所致,异常的α-链是由小肠的浆细胞产生的。IPSID病人往往死于进行性营养不良和衰竭,或死于侵袭性淋巴瘤。
 治疗
治疗
治疗:小肠恶性淋巴瘤除具有肿瘤本身危害性外,还发生严重腹部并发症,如肠梗阻、肠套叠、肠穿孔和消化道出血等。因此在治疗上应争取彻底切除原发病灶,将病变小肠连同肠系膜区域淋巴结一并切除。如肿瘤直径>5cm,侵及肠道外器官者,也应作病变小肠及邻近器官联合脏器切除。对于不能行根治性切除的争取做姑息性手术,切除肠梗阻的肠段,恢复肠道的通畅。个别情况病变难以切除者可做短路手术。术后采取放疗、化疗等综合治疗方法。
1.根治性切除 应切除病变肠管及两端各30cm左右的正常肠管,清扫肠系膜上相应的淋巴结。但有时淋巴结融合成团包绕肠系膜上动、静脉的主干,不能整块切除时,可沿上述血管将淋巴结逐一剥离,在瘤床处标以金属标记,以备术后放疗。
2.放疗 恶性淋巴瘤对放疗较为敏感,手术后均应行放疗,消灭残留组织提高疗效。直线加速器一般在腹部前后进行照射,范围可适当放宽。如情况许可,在四周内给予组织量35~45GY为宜。小肠本身对放射线的耐受性差,剂量过大可造成放射性小肠炎,发生出血、狭窄、穿孔等并发症。
3.化疗 小肠恶性淋巴瘤对化疗亦较敏感。化疗药物的选择和投药方式尚未统一。一般采用氮芥、环磷酰胺(CTX)、长春新碱(VCR)、
多柔比星(
阿霉素,
ADM)、泼尼松(强的松)和丙卡巴肼(甲基苄肼)等疗效较好,常用化疗方案有COP、CHOP、CMOPP等。一般成年人可给长春新碱1mg,静脉注射,1次/周,6~8周为一个疗程。必要时可继续每2周1次,共10次。严重者可加用丙卡巴肼和泼尼松联合用药。在用药期应密切观察血象变化,如白细胞降至3×10
9/L以下应立即停药,等情况改善后再继续用药。
如病人的一般情况良好,可在放疗的同时配合应用化疗,化疗、放疗还可与生物治疗相结合,还应加强全身支持治疗,纠正吸收不良综合征。
4.其他治疗 近年来各种免疫治疗进展较快,除一般的免疫增强剂、转移因子、干扰素等外,阿地白介素(白介素Ⅱ)、LAK细胞及TIL等治疗均有成功的报道。中医中药在扶正、支持病人进行放疗化疗等方面亦有良好的作用。
IPSID可按PSIL治疗,并应对肠道抗感染及驱虫治疗,同时应纠正吸收不良综合征,部分病例可获得缓解。但由于IPSID在小肠的病变范围多数较广泛,能手术切除的可能性较小,仅在个别局限性病变的病例,才能进行手术切除。



 流行病学
流行病学
 病因
病因
 发病机制
发病机制
 临床表现
临床表现
 实验室检查
实验室检查
 其他辅助检查
其他辅助检查
 诊断
诊断
 鉴别诊断
鉴别诊断
 治疗
治疗
 预后
预后
 预防
预防